Ktoré z nasledujúcich častíc majú vlnové vlastnosti? Laboratórna počítačová dielňa
4.4.1. De Broglieho dohad
Dôležitou etapou vo vytváraní kvantovej mechaniky bol objav vlnových vlastností mikročastíc. Myšlienku vlnových vlastností pôvodne navrhol ako hypotézu francúzsky fyzik Louis de Broglie.
Po mnoho rokov bola dominantná teória vo fyzike, že svetlo je elektromagnetické vlnenie. Po práci Plancka (tepelné žiarenie), Einsteina (fotoelektrický efekt) a ďalších sa však ukázalo, že svetlo má korpuskulárne vlastnosti.
Na vysvetlenie niektorých fyzikálnych javov je potrebné uvažovať o svetle ako o prúde fotónových častíc. Korpuskulárne vlastnosti svetla neodmietajú, ale dopĺňajú jeho vlnové vlastnosti.
takže, fotón je elementárna častica svetla s vlnovými vlastnosťami.
Vzorec pre hybnosť fotónu
| . | (4.4.3) |
Podľa de Broglieho je pohyb častice, napríklad elektrónu, podobný vlnovému procesu s vlnovou dĺžkou λ definovanou vzorcom (4.4.3). Tieto vlny sa nazývajú de Broglie vlny. V dôsledku toho môžu častice (elektróny, neutróny, protóny, ióny, atómy, molekuly) vykazovať difrakčné vlastnosti.
K. Davisson a L. Germer ako prví pozorovali difrakciu elektrónov na monokryštáli niklu.
Môže vzniknúť otázka: čo sa deje s jednotlivými časticami, ako vznikajú maximá a minimá pri difrakcii jednotlivých častíc?
Experimenty na difrakcii elektrónových lúčov veľmi nízkej intenzity, teda akoby jednotlivých častíc, ukázali, že v tomto prípade sa elektrón „nešíri“ rôznymi smermi, ale správa sa ako celá častica. Pravdepodobnosť vychýlenia elektrónov v určitých smeroch v dôsledku interakcie s difrakčným objektom je však iná. Elektróny s najväčšou pravdepodobnosťou padnú do miest, ktoré podľa výpočtov zodpovedajú difrakčným maximám, s menšou pravdepodobnosťou padnú do miest s minimami. Vlnové vlastnosti sú teda vlastné nielen skupine elektrónov, ale aj každému elektrónu jednotlivo.
4.4.2. Vlnová funkcia a jej fyzikálny význam
Keďže mikročastica je spojená s vlnovým procesom, ktorý zodpovedá jej pohybu, stav častíc v kvantovej mechanike je opísaný vlnovou funkciou, ktorá závisí od súradníc a času: .
Ak je silové pole pôsobiace na časticu stacionárne, teda nezávislé od času, potom ψ-funkcia môže byť reprezentovaná ako súčin dvoch faktorov, z ktorých jeden závisí od času a druhý od súradníc:
To naznačuje fyzikálny význam vlnovej funkcie:
4.4.3. Vzťah neistoty
Jedným z dôležitých ustanovení kvantovej mechaniky sú vzťahy neurčitosti navrhnuté W. Heisenbergom.
Nech sa súčasne meria poloha a hybnosť častice, pričom nepresnosti v určení úsečky a priemetu hybnosti na os úsečky sa rovnajú Δx a Δр x.
V klasickej fyzike neexistujú žiadne obmedzenia, ktoré by zakazovali súčasné meranie jednej aj druhej veličiny, teda Δx→0 a Δр x→ 0, s akoukoľvek presnosťou.
V kvantovej mechanike je situácia zásadne odlišná: Δx a Δр x, ktoré zodpovedajú súčasnému určeniu x a р x, súvisia so závislosťou
Volajú sa vzorce (4.4.8), (4.4.9). vzťahy neistoty.
Poďme si ich vysvetliť jedným modelovým experimentom.
Pri štúdiu fenoménu difrakcie sa upriamila pozornosť na skutočnosť, že zníženie šírky štrbiny počas difrakcie vedie k zvýšeniu šírky centrálneho maxima. K podobnému javu dôjde pri difrakcii elektrónov štrbinou v modelovom experimente. Zmenšenie šírky štrbiny znamená zmenšenie Δ x (obr. 4.4.1), čo vedie k väčšiemu „rozmazaniu“ elektrónového lúča, teda k väčšej neistote v hybnosti a rýchlosti častíc.

Ryža. 4.4.1 Vysvetlenie vzťahu neistoty.
Vzťah neurčitosti možno znázorniť ako
| , | (4.4.10) |
kde ΔE je neistota energie určitého stavu systému; Δt je časové obdobie, počas ktorého existuje. Vzťah (4.4.10) znamená, že čím kratšia je životnosť ktoréhokoľvek stavu systému, tým je jeho energetická hodnota neistejšia. Energetické hladiny E 1, E 2 atď. majú určitú šírku (obr. 4.4.2)), v závislosti od času zotrvania systému v stave zodpovedajúcom tejto úrovni.

Ryža. 4.4.2 Energetické hladiny E 1, E 2 atď. mať nejakú šírku.
„Rozmazanie“ úrovní vedie k neistote v energii ΔE emitovaného fotónu a jeho frekvencii Δν, keď systém prechádza z jednej energetickej úrovne na druhú:
![]() ,
,
kde m je hmotnosť častice; ; E a E n sú jej celkové a potenciálne energie (potenciálna energia je určená silovým poľom, v ktorom sa častica nachádza, a v stacionárnom prípade nezávisí od času)
Ak sa častica pohybuje len po určitej priamke, napríklad po osi OX (jednorozmerný prípad), potom je Schrödingerova rovnica výrazne zjednodušená a nadobúda tvar
| (4.4.13) |
Jedným z najjednoduchších príkladov použitia Schrödingerovej rovnice je riešenie problému pohybu častíc v jednorozmernej potenciálovej studni.
4.4.5. Aplikácia Schrödingerovej rovnice na atóm vodíka. Kvantové čísla
Popísať stavy atómov a molekúl pomocou Schrödingerovej rovnice je pomerne náročná úloha. Najjednoduchšie sa to rieši pre jeden elektrón nachádzajúci sa v poli jadra. Takéto systémy zodpovedajú atómu vodíka a vodíku podobným iónom (jednorazovo ionizovaný atóm hélia, dvojito ionizovaný atóm lítia atď.). Aj v tomto prípade je však riešenie problému zložité, preto sa obmedzíme len na kvalitatívne podanie problematiky.
Potenciálnu energiu treba najskôr dosadiť do Schrödingerovej rovnice (4.4.12), ktorá pre dva interagujúce bodové náboje - e (elektrón) a Ze (jadro) - umiestnené vo vzdialenosti r vo vákuu, je vyjadrená nasledovne:
Tento výraz je riešením Schrödingerovej rovnice a úplne sa zhoduje so zodpovedajúcim vzorcom Bohrovej teórie (4.2.30)
Obrázok 4.4.3 zobrazuje úrovne možných hodnôt celkovej energie atómu vodíka (E 1, E 2, E 3 atď.) a graf potenciálnej energie E n v závislosti od vzdialenosti r medzi elektrónom a jadro. Ako hlavné kvantové číslo n rastie, r rastie (pozri 4.2.26) a celková (4.4.15) a potenciálna energia majú tendenciu k nule. Kinetická energia má tiež tendenciu k nule. Vytieňovaná plocha (E>0) zodpovedá stavu voľného elektrónu.

Ryža. 4.4.3. Sú zobrazené úrovne možných hodnôt celkovej energie atómu vodíka
a graf potenciálnej energie verzus vzdialenosť r medzi elektrónom a jadrom.
Druhé kvantové číslo je orbitálny l, ktoré pre dané n môže nadobudnúť hodnoty 0, 1, 2, ...., n-1. Toto číslo charakterizuje orbitálny moment hybnosti Li elektrónu vo vzťahu k jadru:
Štvrté kvantové číslo je točiť m s. Môže nadobudnúť iba dve hodnoty (±1/2) a charakterizuje možné hodnoty projekcie elektrónového spinu:
| .(4.4.18) |
Stav elektrónu v atóme s daným n a l označujeme takto: 1s, 2s, 2p, 3s atď. Číslo tu označuje hodnotu hlavného kvantového čísla a písmeno označuje orbitálne kvantové číslo: symboly s, p, d, f zodpovedajú hodnotám l = 0, 1, 2. 3 atď.
Kvantová mechanika je moderná teória, ktorá stanovuje spôsob popisu a zákonitosti pohybu mikročastíc (elementárnych častíc, atómov, molekúl, jadier) a ich systémov. Nezvyčajnosť kvantovo-mechanických konceptov v porovnaní s klasickou fyzikou otvorila obdobie rozpadu základných fyzikálnych modelov, ktoré sa zdali samozrejmé a nezničiteľné. To ovplyvnilo najmä koncepciu častice a princípy jej pohybu.
Táto kapitola predstavuje nielen kvantovú mechaniku, ale aj myšlienky a experimenty, ktoré viedli k tejto teórii. Elektrónová mikroskopia sa považuje za metódu založenú na vlnových vlastnostiach elektrónov.
28.1. DE BROGLIEHO HYPOTÉZA. EXPERIMENTY S DIFRAKCIOU ELEKTRÓNOV A INÝCH ČASTÍC
Dôležitou etapou vo vytváraní kvantovej mechaniky bol objav vlnových vlastností mikročastíc. Myšlienku vlnových vlastností pôvodne predložil ako hypotézu francúzsky fyzik Louis de Broglie (1924) 1 .
Po mnoho rokov bola dominantná teória vo fyzike, že svetlo je elektromagnetické vlnenie. Po práci Plancka (tepelné žiarenie), Einsteina (fotoelektrický efekt) a ďalších sa však ukázalo, že svetlo má korpuskulárne vlastnosti.
1 De Broglieho hypotéza bola formulovaná pred experimentmi potvrdzujúcimi vlnové vlastnosti častíc. De Broglie o tom neskôr, v roku 1936, napísal: „...nemôžeme predpokladať, že elektrón je rovnako duálny ako svetlo? Na prvý pohľad sa tento nápad zdal veľmi odvážny. Koniec koncov, vždy sme si elektrón predstavovali ako elektricky nabitý hmotný bod, ktorý sa riadi zákonmi klasickej dynamiky. Elektrón nikdy jasne nevykazoval vlnové vlastnosti, ako napríklad svetlo vo fenoméne interferencie a difrakcie. Pokus pripísať vlnové vlastnosti elektrónu, keď na to neexistujú žiadne experimentálne dôkazy, by mohol vyzerať ako nevedecká fantázia.
V kap. 24 bolo zaznamenané, že rôntgenová difrakcia je pozorovaná na kryštalických telesách; Preto je pre difrakciu elektrónov potrebné použiť aj kryštalické látky.
K. Davisson a L. Germer prvýkrát pozorovali difrakciu elektrónov z monokryštálu niklu, J.P. Thomson a nezávisle od neho P.S. Tartakovského - na kovovej fólii (polykryštalické telo).
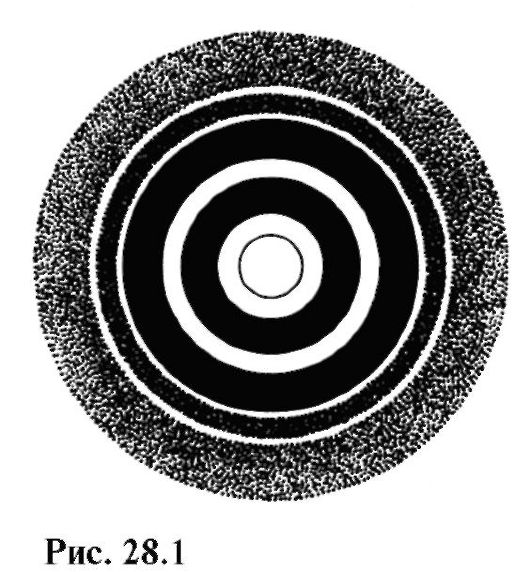
Na obr. Obrázok 28.1 ukazuje elektrónový gram - difrakčný obrazec získaný interakciou elektrónov s polykryštalickou fóliou.
Pri porovnaní tohto obrázku s obr. 24.21 si možno všimnúť podobnosť medzi difrakciou elektrónov a röntgenovým žiarením.
Iné častice, nabité (protóny, ióny atď.), ako aj neutrálne (neutróny, atómy, molekuly), majú tiež schopnosť difrakcie.
Podobne ako pri röntgenovej difrakčnej analýze sa difrakcia častíc môže použiť na určenie usporiadaného alebo neusporiadaného usporiadania atómov a molekúl látky a na odhad parametrov kryštálových mriežok.
V súčasnosti sú široko používané metódy elektrónovej difrakcie (elektrónová difrakcia) a neutrónovej difrakcie (neutrónová difrakcia).
Môžu vzniknúť otázky: čo sa deje s jednotlivými časticami, ako vznikajú maximá a minimá pri difrakcii jednotlivých častíc?
Experimenty o difrakcii elektrónových lúčov veľmi nízkej intenzity, t.j. akoby išlo o samostatné častice, ukázali, že v tomto prípade sa elektrón „nerozšíri“ rôznymi smermi, ale správa sa ako celá častica. Pravdepodobnosť vychýlenia elektrónov v určitých smeroch v dôsledku interakcie s difrakčným objektom je však iná. Elektróny s najväčšou pravdepodobnosťou padnú do miest, ktoré podľa výpočtov zodpovedajú difrakčným maximám, s menšou pravdepodobnosťou padnú do miest s minimami. Vlnové vlastnosti sú teda vlastné nielen skupine elektrónov, ale aj každému elektrónu jednotlivo.
28.2. ELEKTRONOVÝ MIKROSKOP. KONCEPCIA ELEKTRONICKEJ OPTIKY
Vlnové vlastnosti častíc možno využiť nielen na difrakčnú štrukturálnu analýzu, ale aj na získanie zväčšených obrazov objektu.
Z (26.19) vyplýva, že medza rozlíšenia optického mikroskopu je určená najmä limitnou vlnovou dĺžkou svetla vnímaného ľudským okom. Dosadením hodnoty de Broglieho vlnovej dĺžky (28.3) do tohto vzorca nájdeme medzu rozlíšenia elektrónového mikroskopu, v ktorom je obraz objektu tvorený elektrónovými lúčmi:
Ako môžete ľahko vidieť, limit rozlíšenia z Elektrónový mikroskop závisí od urýchľovacieho napätia a dá sa dosiahnuť, že je oveľa nižšie a rozlíšenie oveľa väčšie ako u optického mikroskopu.
Elektrónový mikroskop a jeho jednotlivé prvky sú svojím účelom podobné optickému mikroskopu, preto na vysvetlenie jeho štruktúry a princípu činnosti použijeme analógiu. Schémy oboch mikroskopov sú na obr. 28,2 (a - optický; b - elektronický).
V optickom mikroskope nosič informácie o objekte AB je fotón, svetlo. Zdrojom svetla býva žiarovka /. Po interakcii s objektom (absorpcia, rozptyl, difrakcia) sa fotónový prúd transformuje a obsahuje informácie o objekte. Fotónový tok sa vytvára pomocou optických zariadení, najmä šošoviek: kondenzor 3, objektív 4, okulár 5. Obraz A 1 B 1 je zaznamenaný okom 7 (alebo fotografickou doskou, fotoluminiscenčnou clonou atď.).
V elektrónovom mikroskope je nositeľom informácie o objekte elektrón a zdrojom elektrónov je vyhrievaná katóda 1. Urýchlenie elektrónov a vznik lúča sa uskutočňuje pomocou zaostrovacej elektródy a anódy - systému nazývané elektrónové delo 2. Po interakcii s objektom (hlavne rozptylu) sa tok elektrónov transformuje a obsahuje informácie o subjekte. K tvorbe toku elektrónov dochádza pod vplyvom elektrického poľa (systém elektród a kondenzátorov) a magnetického poľa (systém

ma cievky s prúdom). Tieto systémy sa nazývajú elektronické šošovky analogicky s optickými šošovkami, ktoré tvoria svetelný tok (3 - kondenzátor; 4 - elektronický, slúžiaci ako šošovka, 5 - projekcia). Obraz sa zaznamenáva na fotografickú platňu citlivú na elektróny alebo katodoluminiscenčnú obrazovku 6.
Na odhadnutie limitu rozlíšenia elektrónového mikroskopu dosadíme do vzorca (28.4) urýchľovacie napätie 100 kV a uhlovú apertúru rádovo 10 -2 rad (približne tieto uhly sa používajú v elektrónovej mikroskopii). Potom dostaneme z ~ 0,1 nm, čo je stokrát lepšie ako optické mikroskopy. Použitie urýchľovacieho napätia väčšieho ako 100 kV, hoci zvyšuje rozlíšenie, je spojené s určitými ťažkosťami, najmä sa vyskytuje
zničenie skúmaného objektu elektrónmi s vysokou rýchlosťou. V praxi je možné aj s najlepším elektrónovým mikroskopom dosiahnuť hranicu rozlíšenia rádovo 10 -10 m; to je stokrát lepšie ako optické mikroskopy.
Medzi výhody elektrónového mikroskopu patrí vysoká rozlišovacia schopnosť umožňujúca skúmanie veľkých molekúl, možnosť v prípade potreby meniť urýchľovacie napätie a následne aj hranicu rozlišovacej schopnosti a pomerne pohodlné riadenie toku elektrónov pomocou magnetických a elektrických polí.
Uveďme niektoré vlastnosti činnosti elektrónového mikroskopu. V tých častiach, kde lietajú elektróny, musí byť vákuum, pretože inak kolízia elektrónov s molekulami vzduchu (plynu) povedie k skresleniu obrazu. Táto požiadavka na elektrónovú mikroskopiu komplikuje výskumný postup a robí zariadenie ťažkopádnejším a nákladnejším. Vákuum skresľuje prirodzené vlastnosti biologických objektov a v niektorých prípadoch ich ničí alebo deformuje.
Na skúmanie pod elektrónovým mikroskopom sú vhodné len veľmi tenké rezy, pretože elektróny sú látkou silne absorbované a rozptýlené. Preto je v niektorých prípadoch vhodné urobiť odtlačok povrchu skúmaného objektu na tenkú vrstvu plastu. Tento postup sa nazýva replikácia a nazýva sa plastická kópia povrchu replika.

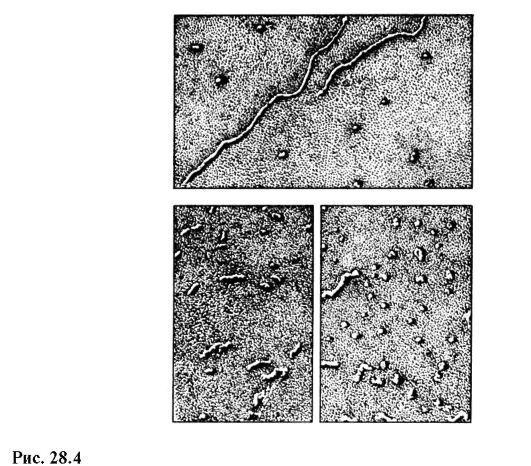
Moderný domáci elektrónový mikroskop EVM-100 LM (obr. 28.3) poskytuje maximálne 600 000-násobné zväčšenie a garantovanú hranicu rozlíšenia 3? 10 -10 m. Obrázok 28.4 ukazuje fotografie molekúl RNA v rôznych stavoch získaných na elektrónovom mikroskope so 100 000-násobným zväčšením.
Prítomnosť vlnových a korpuskulárnych vlastností vo fotónoch, elektrónoch a iných časticiach umožňuje rozšíriť množstvo princípov a zákonov optiky na popis pohybu nabitých častíc v elektrických a magnetických poliach.
Táto analógia umožnila identifikovať sa ako samostatný oddiel elektronická optika - oblasť fyziky, ktorá študuje štruktúru zväzkov nabitých častíc interagujúcich s elektrickými a magnetickými poľami. Rovnako ako konvenčnú optiku, aj elektronickú optiku možno rozdeliť na geometrický (radiálne) a mávať(fyzické).
V rámci geometrickej elektrónovej optiky je popísaný najmä pohyb nabitých častíc v elektrických a magnetických poliach. Schematické znázornenie konštrukcie obrazu v elektrónovom mikroskope (pozri obr. 28.2, b) je založené na geometrickej elektrónovej optike.
Prístup vlnovej elektrónovej optiky je nevyhnutný v prípade, keď sa prejavia vlnové vlastnosti nabitých častíc. Dobrým príkladom je zistenie rozlíšenia (limit rozlíšenia) uvedeného na začiatku odseku.
28.3. VLNOVÁ FUNKCIA A JEJ FYZIKÁLNY VÝZNAM
Keďže mikročastica je spojená s vlnovým procesom, ktorý zodpovedá jej pohybu, stav častíc v kvantovej mechanike je opísaný vlnovou funkciou závislou od súradníc a času: ψ(χ, y, z, t).
Ak je silové pole pôsobiace na časticu stacionárne, t.j. nezávisle od času, potom môže byť ψ-funkcia reprezentovaná ako súčin dvoch faktorov, z ktorých jeden závisí od času a druhý od súradníc:
Ďalej budeme uvažovať iba o stacionárnych stavoch; ψ-funkcia je pravdepodobnostná charakteristika stavu častice. Vysvetlime si význam tohto tvrdenia.
Vyberme dostatočne malý objem v priestore dV= dxdjdz, v rámci ktorého možno hodnoty ψ-funkcie považovať za identické. Pravdepodobnosť nájdenia dW Bčastice v tomto objeme sú úmerné objemu a závisia od štvorcového modulu ψ-funkcie:

Kvadratický modul vlnovej funkcie sa rovná hustote pravdepodobnosti, t.j. pomer pravdepodobnosti nájdenia častice v objeme k tomuto objemu.
Integrovaním výrazu (28.6) nad určitým objemom V zistíme pravdepodobnosť nájdenia častice v tomto objeme:
28.4. VZŤAHY NEISTOTY
Jedným z dôležitých ustanovení kvantovej mechaniky sú vzťahy neurčitosti navrhnuté W. Heisenbergom.
Nech sa súčasne zmeria poloha a hybnosť častice, pričom nepresnosti v určení úsečky a priemetu hybnosti na os úsečky sú rovné Δχ a Δр x.

1 V skutočnosti nie je možné takýto experiment uskutočniť, keďže rozmery medzery musia byť rádovo v atómoch, preto je opísaný istý myšlienkový experiment.

Riešenie (28.11) znamená, že čím kratšia je životnosť ktoréhokoľvek stavu systému, tým je jeho energetická hodnota neistejšia. Energetické hladiny E 1, E 2 atď. majú určitú šírku (obr. 28.6), v závislosti od času zotrvávania systému v stave zodpovedajúcom tejto úrovni.
„Rozmazanie“ úrovní vedie k neistote v energii AE emitovaného fotónu a jeho frekvencii Ay, keď systém prechádza z jednej energetickej úrovne na druhú:
Keďže stav mikročastice je opísaný ψ-funkciou, je potrebné uviesť metódu na nájdenie tejto funkcie s prihliadnutím na vonkajšie podmienky. Je to možné vďaka vyriešeniu základnej rovnice kvantovej mechaniky, ktorú navrhol E. Schrödinger (1926). Takáto rovnica je postulovaná v kvantovej mechanike rovnakým spôsobom, ako je postulovaný druhý Newtonov zákon v klasickej mechanike.
Vo vzťahu k stacionárnym stavom možno Schrödingerovu rovnicu zapísať takto:
To sa prejavuje rozšírením spektrálnych čiar.
28.5. SCHRÖDINGEROVÁ ROVNICE. ELEKTRÓN V POTENCIÁLNEJ STUDE
Kde m- hmotnosť častíc; E a E p - jeho celková a potenciálna energia (potenciálna energia je určená silovým poľom, v ktorom sa častica nachádza, a v stacionárnom prípade nezávisí od času).
Ak sa častica pohybuje len po určitej priamke, napríklad po osi X(jednorozmerný prípad), potom je Schrödingerova rovnica výrazne zjednodušená a nadobúda tvar:
Jedným z najjednoduchších príkladov použitia Schrödingerovej rovnice je riešenie problému pohybu častíc v jednorozmernej potenciálovej studni.
Nechajte elektrón pohybovať sa pozdĺž osi X len v rámci 0< X < l(obr. 28.7). To znamená, že v zadanom intervale je funkcia ψ nenulová a mimo intervalu (x<0, X>l) sa rovná nule.
Keďže silové polia nepôsobia na časticu vo zvolenom intervale, jej potenciálna energia môže mať ľubovoľnú konštantnú hodnotu (najvýhodnejšie je vziať E p= 0). Mimo tohto intervalu nie je žiadny elektrón, takže jeho potenciálna energia by sa mala považovať za nekonečne veľkú. Na obr. Na obrázku 28.7 je znázornená grafická závislosť E p = D x). Interval 0< X < l, удовлетворяющий сформулированным выше условиям, называют одномерной прямоугольной потенциальной ямой с бесконечно высокими стенками. С учетом E p= 0 Schrödingerova rovnica (28.14) pre interval 0< X < l má tvar:

Táto rovnica je podobná diferenciálnej rovnici harmonického kmitania (pozri 7.1), ktorej riešením je:

V prvom rade je pozoruhodné, že riešenie Schrödingerovej rovnice pre elektrón v potenciálovej studni bez akýchkoľvek ďalších postulátov vedie k diskrétnym kvantovaným energetickým hodnotám:

Z (28.21) je zrejmé, že pre nejakú pevnú hodnotu n diskrétnosť, t.j. Čím väčšia je veľkosť potenciálnej studne, tým menší je rozdiel v energiách susedných úrovní. Vypočítajme teda napríklad dva prípady s n = 1:
1) l= 5? 10 -10 m, čo približne zodpovedá veľkosti atómu; Potom ΔΕ = 4,5 eV. To sa rádovo zhoduje s hodnotami získanými pre atóm vodíka podľa Bohrovej teórie;
2) l= 10 -1 m, čo vlastne zodpovedá takej šírke potenciálovej jamy, že elektrón možno považovať za voľný; kde ΔΕ = 1.1? 10-16 eV. Tu je diskrétnosť zanedbateľná a prakticky môžeme predpokladať, že energia elektrónu sa plynule mení.
Umocnením (28.20) získame hustotu pravdepodobnosti |ψ| 2 nájdenie elektrónu v rôznych bodoch potenciálovej studne. Na obr. Obrázok 28.9 ukazuje grafickú závislosť |ψ| 2 od χ pod rôznymi diskrétnymi stavmi, t.j. rôzne kvantové čísla. Ako vidno z obrázku, elektrón sa môže nachádzať na rôznych miestach v potenciálovej studni s rôznou pravdepodobnosťou. Existujú body, v ktorých je pravdepodobnosť nájdenia elektrónu nulová. To sa výrazne líši od koncepcií klasickej fyziky, podľa ktorej je prítomnosť častice na rôznych miestach potenciálnej jamy rovnako pravdepodobná (obr. 28.10) a nemožno jamu rozdeliť bodmi, v ktorých prítomnosť častice je vylúčené.
Schrödingerova rovnica sa dá aplikovať aj na zložitejšie silové polia, ako je elektrón v atóme. To povedie k ďalším matematickým ťažkostiam, ale nezmení hlavné črty

atómové systémy: diskrétnosť energetických stavov, pravdepodobnostné úsudky o umiestnení elektrónu, zvláštna závislosť |ψ| 2 zo súradníc atď.
28.6. APLIKÁCIA SCHRÖDINGEROVEJ ROVNICE NA ATÓM VODÍKA. KVANTOVÉ ČÍSLA
Popísať stavy atómov a molekúl pomocou Schrödingerovej rovnice je pomerne náročná úloha. Najjednoduchšie sa to rieši pre jeden elektrón nachádzajúci sa v poli jadra. Takéto systémy zodpovedajú atómu vodíka a vodíku podobným iónom (jednorazovo ionizovaný atóm hélia, dvojito ionizovaný atóm lítia atď.). Riešenie problému je však aj v tomto prípade nad rámec nášho kurzu, preto sa obmedzíme len na kvalitatívne podanie problematiky.
Potenciálna energia by sa mala najskôr nahradiť Schrödingerovou rovnicou (28.13), ktorá je pre dva interagujúce bodové náboje e(elektrón) a Ze(jadro), - umiestnené na diaľku r vo vákuu sa vyjadruje takto:
Vzhľadom na stredovú symetriu poľa vytvoreného jadrom je vhodnejšie riešiť problém nie v karteziánskych pravouhlých súradniciach, ale v sférických r, θ a p.
Riešenie Schrödingerovej rovnice sa nachádza ako súčin troch funkcií, z ktorých každá závisí od jednej premennej:
Tak ako pre elektrón v pravouhlej potenciálovej studni s nekonečne vysokými stenami viedli okrajové podmienky ku konkrétnym možným hodnotám ψ a energie, tak v potenciálovej jame zodpovedajúcej atómu vodíka vedú fyzikálne podmienky k možným hodnotám f1, f 2, f 3 a teda ψ-funkcia. Prejavuje sa tu aj hlavná črta kvantových mechanických systémov – diskrétnosť stavov.
Diskrétnosť matematicky spočíva v tom, že ktorákoľvek z funkcií rovnice (28.23) má celý súbor (spektrum) riešení, z ktorých každé zodpovedá určitému kvantovému číslu. Na rozdiel od pravouhlej potenciálovej studne s nekonečne vysokými stenami je stav elektrónu v atóme charakterizovaný nie jedným, ale niekoľkými kvantovými číslami 1 . Prvým je hlavné kvantové číslo P - 1, 2, 3... Určuje energetické hladiny elektrónu podľa zákona:

Tento výraz je riešením Schrödingerovej rovnice a úplne sa zhoduje so zodpovedajúcim vzorcom Bohrovej teórie (pozri 28.7).
Na obr. Obrázok 28.11 zobrazuje úrovne možných hodnôt celkovej energie atómu vodíka (E 1, E 2, E 3 atď.) a graf potenciálnej energie E P v závislosti od vzdialenosti r medzi elektrónom a jadrom [pozri (28,22)]. S rastúcim hlavným kvantovým číslom P zvyšuje r[pozri napríklad (28.33)] a doplňte [pozri. (28.24)] a potenciálna energia má tendenciu k nule. Kinetická energia má tiež tendenciu k nule. Vytieňovaná plocha (E >0) zodpovedá stavu voľného elektrónu.
1 Vo všeobecnosti sú kvantové čísla celočíselné (0, 1, 2...) alebo polovičné (1/2, 3/2, 5/2...) čísla, ktoré definujú možné diskrétne hodnoty fyzikálnych veličín, ktoré charakterizovať kvantové systémy a elementárne častice.

1 Prítomnosť spinu v časticiach nevyplýva zo Schrödingerovej rovnice.
s týmto výpočtom: strávila viac času na miestach s vyššou hustotou pravdepodobnosti, menej času na miestach s nižšou hustotou pravdepodobnosti. V dôsledku expozície na fotografickom filme sa získali oblasti rôznych intenzít, ktoré ilustrujú distribúciu elektrónu v atóme. Z obrázkov je zrejmé, aký svojvoľný a dokonca nesprávny je pojem „obežná dráha“ vo vzťahu k pohybu elektrónu.
Spin a orbitálne magnetické momenty sa navzájom ovplyvňujú, čo mení systém energetických hladín atómu v porovnaní s tým, čo by bolo bez takejto interakcie. Hovorí sa, že interakcie spin-orbita vedú k jemnej štruktúre energetických hladín. Ak je významný, potom je potrebné vziať do úvahy celkový moment hybnosti elektrónu - orbital plus spin. Navyše namiesto toho m l A pani použite iné kvantové čísla: j A nij.
Kvantové číslo j- orbital plus spin - určuje diskrétne hodnoty celkového momentu hybnosti L elektrón:

Magnetické kvantové číslo m) charakterizuje možné projekcie celkového momentu hybnosti do nejakého ľubovoľne zvoleného smeru Z:
Za danú l kvantové číslo j nadobúda dve hodnoty: ±1/2
(Tabuľka 28.1).
Tabuľka 28.1

Za danú j kvantové číslo nij má hodnoty 2j + 1: -J J + 1 ... + j.
28.7. KONCEPCIA O BOHROVEJ TEÓRII
Ešte pred vytvorením kvantovej mechaniky v roku 1913 dánsky fyzik N. Bohr navrhol teóriu atómu vodíka a vodíku podobných iónov, ktorá vychádzala z jadrového modelu atómu a jeho dvoch postulátov. Bohrove postuláty nezapadali do rámca klasickej fyziky.
Podľa prvého postulátu môžu atóm a atómové systémy zostať dlhý čas iba v určitých stacionárnych stavoch. V takýchto stavoch atóm nevyžaruje ani neabsorbuje energiu. Stacionárne stavy zodpovedajú diskrétnym energetickým hodnotám: E 1, E 2...
Akákoľvek zmena energie atómu alebo atómového systému je spojená s náhlym prechodom z jedného stacionárneho stavu do druhého.
Podľa druhého postulátu, keď atóm prechádza z jedného stavu do druhého, atóm emituje alebo absorbuje fotón, ktorého energia je určená rovnicou (29.1).
Prechod zo stavu s vyššou energiou do stavu s nižšou energiou je sprevádzaný emisiou fotónu. Opačný proces je možný, keď je fotón absorbovaný.
Podľa Bohrovej teórie elektrón v atóme vodíka rotuje po kruhovej dráhe okolo jadra. Zo všetkých možných dráh zodpovedajú stacionárne stavy iba tým, pre ktoré sa moment hybnosti rovná celému číslu h/(2π):
(n = 1, 2, 3...), (28,31)
Kde m- hmotnosť elektrónov; υ η - jeho rýchlosť na n-tej obežnej dráhe; rn- jeho polomer. Elektrón rotujúci po kruhovej dráhe v atóme je vystavený Coulombovej sile príťažlivosti od kladne nabitého jadra, ktorá sa podľa druhého Newtonovho zákona rovná súčinu hmotnosti elektrónu a dostredivého zrýchlenia (označenie uvedené pre vákuum ):

Napriek veľkému úspechu Bohrovej teórie sa čoskoro prejavili jej nedostatky. V rámci tejto teórie teda nebolo možné vysvetliť rozdiel v intenzitách spektrálnych čiar, t.j. odpovedať na otázku, prečo sú niektoré energetické prechody pravdepodobnejšie ako iné. Bohrova teória neodhalila spektrálne vzorce zložitejšieho atómového systému – atómu hélia (dva elektróny rotujúce okolo jadra).
Nevýhodou Bohrovej teórie bola jej nejednotnosť. Táto teória nebola ani klasická, ani kvantová, spájala ustanovenia zásadne odlišných teórií: klasickej a kvantovej fyziky. Takže napríklad v Bohrovej teórii sa verí, že elektrón rotuje v atóme na určitej dráhe (klasické koncepty), ale zároveň nevyžaruje elektromagnetickú vlnu (kvantové koncepty).
V prvej štvrtine tohto storočia sa ukázalo, že Bohrova teória musí byť nahradená inou teóriou atómu. Objavila sa kvantová mechanika.
28.8. ELEKTRONOVÉ PLÁŠKY KOMPLEXNÝCH ATÓMOV
Kvantové čísla, ktoré popisujú stav elektrónu v atóme vodíka, sa používajú na aproximáciu stavu jednotlivých elektrónov v komplexných atómoch. Mali by sa však vziať do úvahy aspoň dva významné rozdiely medzi komplexnými atómami a atómom vodíka:
1) v zložitých atómoch závisí energia elektrónov v dôsledku ich interakcie nielen od n, ale aj od /;
2) rozdiel je spôsobený Pauliho princípom, podľa ktorého atóm nemôže mať dva (alebo viac) elektrónov so štyrmi rovnakými kvantovými číslami.
Keď sa vytvorí elektrónová konfigurácia zodpovedajúca normálnemu stavu, každý elektrón atómu má tendenciu mať najnižšiu energiu. Ak by nebol Pauliho princíp, potom by sa všetky elektróny nachádzali na najnižšej energetickej úrovni. V skutočnosti, až na niektoré výnimky, elektróny zaberajú sekvenciu stavov uvedenú pre atóm vodíka v tabuľke. 29.
Elektróny s rovnakým hlavným kvantovým číslom tvoria vrstvu. Vrstvy sú tzv TO, L, M, N atď. v súlade s n= 1, 2, 3, 4... Elektróny s rovnakými pármi hodnôt n A / , sú súčasťou obalu, ktorý sa stručne označuje rovnakým spôsobom ako zodpovedajúce stavy pre elektrón atómu vodíka: 1s, 2s, 2^ atď. Takže napríklad volajú 2s obal, 2s elektróny atď.
Počet elektrónov v obale je uvedený vpravo hore vedľa symbolického označenia obalu, napríklad 2p 4.
Distribúcia elektrónov v obaloch v atóme (elektronické konfigurácie) sa zvyčajne označuje takto: pre dusík 1s 2, 2 s 2, 2p 3, pre vápnik 1s 2, 2s 2, 2p 6, 3s 2, 3p 6, 4s 2 atď.
Keďže energia elektrónov zložitých atómov závisí nielen od n, ale aj od l, potom ku konštrukcii periodickej tabuľky nedochádza vždy postupným vypĺňaním vrstiev, keď sa atóm stáva zložitejším. Napríklad v draslíku (Z = 19) namiesto naplnenia vrstvy M(možno tam boli 1s 2, 2s 2, 2^6, 3s 2, 3p 6, 3a 1) začína plnenie vrstvy N a vytvorí sa nasledujúca elektronická konfigurácia: 1 s2, 2s 2, 2R 6, 3 s 2, 3p 6, 4 s 1.
Podobné odchýlky od pravidelného plnenia vrstiev existujú aj v iných prvkoch.
Všeobecné pravidlo je vždy splnené: elektróny nevybudeného atómu zaberajú stav s najnižšou energiou a v súlade s Pauliho princípom. Na obr. Obrázok 28.13 schematicky ukazuje, bez ohľadu na mierku, energetické stavy komplexného atómu a zodpovedajúci počet elektrónov.
Na záver poznamenávame, že stav viacelektrónového atómu ako celku je určený nasledujúcimi kvantovými číslami: L- celkový orbitálny moment atómu, ktorý nadobúda hodnoty 0, 1, 2, 3 atď. 1; J- celkový moment atómu, ktorý môže nadobúdať hodnoty s intervalom jedna od |L - S| na |L + S |; S- výsledný spinový moment atómu; magnetické m J, ktorý určuje diskrétne hodnoty projekcie celkového momentu atómu na určitú os Z:

Za danú Jm J trvá 2 J+ 1 hodnoty:
-J J+ 1 ... +J.
1 Toto označenie by sa nemalo zamieňať s názvom elektronickej vrstvy L a s celkovým momentom hybnosti elektrónu.
28.9. ENERGETICKÁ HLADINA MOLEKÚL
Keďže molekuly sa skladajú z atómov, vnútromolekulový pohyb je zložitejší ako vnútroatómový. V molekule okrem pohybu elektrónov voči jadrám dochádza k vibračnému pohybu atómov okolo ich rovnovážnej polohy (vibrácia jadier spolu s elektrónmi, ktoré ich obklopujú) a k rotačnému pohybu molekuly ako celku.
Elektronické, vibračné a rotačné pohyby molekuly zodpovedajú trom typom energetických úrovní: Eel, Ecol a Etemp. Podľa kvantovej mechaniky má energia všetkých typov pohybu v molekule iba diskrétne hodnoty (kvantované). Predstavme približne celkovú energiu E molekuly súčtom kvantovaných energií rôznych typov:
E= E el + E počet + E čas. (28,37)
Na obr. 28.14 schematicky znázorňuje systém úrovní molekuly: ďaleko od seba úrovne elektronickej energie A" A A"", pre ktoré E coll = E vr = 0; bližšie umiestnené úrovne vibrácií v" , v"", pre nich E vr = 0; najbližšie umiestnené rotačné úrovne J" A J"" s rôznymi hodnotami času E.
Vzdialenosť medzi úrovňami elektronickej energie je rádovo niekoľko elektrónvoltov, medzi susednými vibračnými úrovňami 10-2-10-1 eV, medzi susednými rotačnými úrovňami 10-5-10-3 eV.

Nedostatky Bohrovej teórie poukazovali na potrebu revidovať základy kvantovej teórie a predstavy o podstate mikročastíc (elektróny, protóny atď.). Vznikla otázka, nakoľko komplexné je znázornenie elektrónu vo forme malej mechanickej častice, charakterizovanej určitými súradnicami a určitou rýchlosťou.
Už vieme, že v optických javoch sa pozoruje určitý druh dualizmu. Spolu s javmi difrakcie a interferencie (vlnové javy) sú pozorované aj javy, ktoré charakterizujú korpuskulárnu povahu svetla (fotoelektrický jav, Comptonov jav).
V roku 1924 to predpokladal Louis de Broglie dualizmus nie je znakom len optických javov ,ale má univerzálny charakter. Častice hmoty majú tiež vlnové vlastnosti .
„V optike,“ napísal Louis de Broglie, „bola korpuskulárna metóda vyšetrenia po celé storočie príliš zanedbávaná v porovnaní s vlnovou; neurobila sa v teórii hmoty opačná chyba?" Za predpokladu, že častice hmoty spolu s korpuskulárnymi vlastnosťami majú aj vlnové vlastnosti, de Broglie preniesol na častice hmoty rovnaké pravidlá prechodu z jedného obrazu na druhý, ktoré platia v prípade svetla.
Ak má fotón energiu a hybnosť, tak častica (napríklad elektrón) pohybujúca sa určitou rýchlosťou má vlnové vlastnosti, t.j. pohyb častice možno považovať za pohyb vlny.
Podľa kvantovej mechaniky voľný pohyb častice s hmotnosťou m a hybnosť (kde υ je rýchlosť častice) môže byť reprezentovaná ako rovinná monochromatická vlna ( de Broglieho vlna) s vlnovou dĺžkou
| (3.1.1) |
šíri v rovnakom smere (napríklad v smere osi X) v ktorom sa častica pohybuje (obr. 3.1).

Závislosť vlnovej funkcie od súradnice X je daný vzorcom
| , | (3.1.2) |
Kde - vlnové číslo ,A vlnový vektor smerujúce k šíreniu vlny alebo pozdĺž pohybu častice:
| . | (3.1.3) |
teda monochromatický vlnový vektor spojené s voľne sa pohybujúcou mikročasticou, úmerné jeho hybnosti alebo nepriamo úmerné vlnovej dĺžke.
Keďže kinetická energia relatívne pomaly sa pohybujúcej častice je , možno vlnovú dĺžku vyjadriť aj prostredníctvom energie:
| . | (3.1.4) |
Keď častica interaguje s nejakým objektom - s kryštálom, molekulou atď. – mení sa jej energia: pridáva sa k nej potenciálna energia tejto interakcie, čo vedie k zmene pohybu častice. V súlade s tým sa mení povaha šírenia vlny súvisiacej s časticami, a to sa deje v súlade s princípmi spoločnými pre všetky vlnové javy. Preto sa základné geometrické obrazce difrakcie častíc nelíšia od obrazcov difrakcie akýchkoľvek vĺn. Všeobecnou podmienkou pre difrakciu vĺn akejkoľvek povahy je porovnateľnosť dĺžky dopadajúcej vlny. λ so vzdialenosťou d medzi rozptylovými centrami: .
Hypotéza Louisa de Broglieho bola revolučná, dokonca aj na tú revolučnú dobu vo vede. Čoskoro to však potvrdili mnohé experimenty.
KLASICKÉ MODELY ATÓMOV A ICH NEVÝHODY.
Nápady o čom atómy nie sú nedeliteľné častice a obsahujú ako zložky
elementárne náboje častíc boli najprv vyjadrené na konciXIX storočia Termín „elektrón“ navrhol v roku 1881 anglický fyzik GeorgeNariekať. V roku 1897 bola elektrónová hypotéza experimentálnapotvrdenie v štúdiách Emila Wicherta a Josepha Jana Thomsona. Od tohto momentu sa začalo s tvorbou rôznych elektronických modelovatómov a molekúl.Prvý Thomsonov model predpokladal, že kladný náboj je rovnomernýrozptýlené po celom atóme a do neho, ako hrozienka v žemli,elektróny sú rozptýlené.Rozpor medzi týmto modelom a experimentálnymi údajmi sa ukázal byť jasnýpo experimente v roku 1906 Ernesta Rutherforda, ktorý skúmal
proces rozptylu častíc alfa atómami. Zo skúseností, ktoré ste urobili,že kladný náboj sa koncentruje vo vnútri útvaru, je podstatnémenšia ako veľkosť atómu. Tento útvar sa nazýval atómovýjadro, ktorého rozmery boli 1 o-12 cm a rozmery atómu boli 1 o-v cm.
V súlade s klasickými koncepciami elektromagnetizmumedzi každým elektrónom a jadrom musí byť Coulombova silapríťažlivosť. Závislosť tejto sily od vzdialenosti by mala byť nasledovnárovnako ako v zákone univerzálnej gravitácie. Preto ten pohyb
elektróny v atóme by mali byť podobnéale pohyb planét slnečnej sústavy.Tak sa zrodil planetárny modelRutherfordov atóm.Ďalší výskum udržateľnostiatom dal ohromujúci výsledok:výpočty ukázali, že počas1 o-9 s musí elektrón dopadnúť k jadru
v dôsledku straty energie v dôsledku žiarenia. Navyše, takýto model dalskôr spojité ako diskrétne emisné spektrá atómov.
TEÓRIA ATÓMU BÓRU.
Ďalším dôležitým krokom v Vývojom teórie atómov sa zaoberal Niels Bohr.
Najdôležitejšia hypotéza, ktorú predložil Bohr v r 1913 sa objavila hypotéza o diskrétnej štruktúre
energetické hladiny elektrónu v atóme. Táto pozícia ilustrované na energetike
diagramy. Tradične na energetike diagramy, energia je uložená vertikálne
osi Rozdiel medzi pohybom telesa v gravitačnom poliz pohybu elektrónu v atómev súlade s Bohrovou hypotézou pozostáva zže energia tela sa môže neustále meniť,a energia elektrónov pri záporných hodnotáchmôže nadobudnúť množstvo diskrétnych hodnôt,znázornené na obrázku segmentmi modrej farbyfarby. Tieto diskrétne hodnoty boli tzvenergetické hladiny alebo, inými slovami, energiaúrovne. Samozrejme, myšlienka diskrétnych úrovní energiebol prevzatý z Planckovej hypotézy. Zmena energieelektrón v súlade s Bohrovou teóriou moholvyskytujú sa iba v skokoch (z jednej energetickej hladinyďalší). Bohrova teória dokonale vysvetlila lineárny charakter
atómové spektrá. Pri otázke na dôvod diskrétnosti
teória v skutočnosti neposkytla odpoveď.
VLNY HMOTY.
Ďalším krokom vo vývoji teórie mikrosveta bolo vyrobil Louis de Broglie. V roku 1924 to navrholpohyb mikročastíc by sa nemal označovať ako klasický mechanický
pohyb, ale ako nejaký vlnový pohyb. Vyplýva to zo zákonov vlnový pohyb, treba získať recepty na výpočet rozdielovžiadne pozorovateľné množstvá. Takže vo vede spolu s elektromagnetickými vlnamipolia sa objavili vlny hmoty.Hypotéza o vlnovej povahe pohybu častíc bola rovnako odvážna akoako aj Planckova hypotéza o vlastnostiach diskrétneho poľa. experiment,priame potvrdenie hypotézyBroglie, bol dodaný až v roku 1927.V tomto experimente to bolo pozorovanéelektrónová difrakcia na kryštáli,podobne ako elektromagnetická difrakcia vlny. Hypotéza o vlnách hmoty bola povolenávysvetliť diskrétnu povahu
energetické hladiny. Z teórie vlny, bolo známe, že vlna obmedzená v priestore má vždydiskrétne frekvencie. Príkladom je vlna v takomto muzikálinástroj ako flauta. Frekvencia zvuku je v tomto prípade určenározmery priestoru, ktorým je vlna obmedzená (rozmery flauty).Ukazuje sa, že ide o všeobecnú vlastnosť vĺn.Ale v súlade s Planckovou hypotézou, frekvencia elektromagnetického kvantavlny sú úmerné energii kvanta. V dôsledku toho energia elektrónovmusí nadobúdať diskrétne hodnoty.De Broglieho nápad sa ukázal ako veľmi plodný, hoci, ako už bolo spomenuté,priamy experiment potvrdzujúci vlnové vlastnosti elektrónu, bola vykonaná až v roku 1927. V roku 1926 Erwin Schrödinger odvodil rovnicu,ktorým sa musí elektrónová vlna podriadiť a po vyriešení tohtorovnice aplikovanej na atóm vodíka, získali všetky výsledky, ktoréBohrova teória bola schopná poskytnúť. V skutočnosti to bol začiatokmoderná teória popisujúca procesy v mikrokozme, od rvlnová rovnica bola ľahko zovšeobecnená pre širokú škálu systémov - multielektrónatómy, molekuly, kryštály.Rozvoj teórie viedol k pochopeniu, že vlna korešponduječastice, určuje pravdepodobnosť nájdenia častice v danom bodepriestor. Takto vstúpil pojem pravdepodobnosti do fyziky mikrosveta.Podľa novej teórie vlna zodpovedajúca častici úplne určujepohyb častíc. Ale všeobecné vlastnosti vĺn sú také, že vlnanemožno lokalizovať v žiadnom bode priestoru, t.j. nezmyselnéhovoriť o súradniciach častice v danom časovom okamihu.Dôsledkom toho bolo úplné vylúčenie takých z fyziky mikrosvetapojmy ako trajektória častíc a dráhy elektrónov vatóm. Krásny a vizuálny planetárny model atómu, ako sa ukázalo,
