Které z následujících částic mají vlnové vlastnosti? Laboratorní počítačová dílna
4.4.1. De Broglieho domněnka
Důležitou etapou ve vzniku kvantové mechaniky byl objev vlnových vlastností mikročástic. Myšlenku vlnových vlastností původně navrhl jako hypotéza francouzský fyzik Louis de Broglie.
Po mnoho let převládala ve fyzice teorie, že světlo je elektromagnetické vlnění. Po práci Plancka (tepelné záření), Einsteina (fotoelektrický jev) a dalších se však ukázalo, že světlo má korpuskulární vlastnosti.
Pro vysvětlení některých fyzikálních jevů je nutné uvažovat světlo jako proud fotonových částic. Korpuskulární vlastnosti světla neodmítají, ale doplňují jeho vlnové vlastnosti.
Tak, foton je elementární částice světla s vlnovými vlastnostmi.
Vzorec pro hybnost fotonu
| . | (4.4.3) |
Podle de Broglieho je pohyb částice, například elektronu, podobný vlnovému procesu o vlnové délce λ definované vzorcem (4.4.3). Tyto vlny se nazývají de Broglie vlny. V důsledku toho mohou částice (elektrony, neutrony, protony, ionty, atomy, molekuly) vykazovat difrakční vlastnosti.
K. Davisson a L. Germer jako první pozorovali difrakci elektronů na monokrystalu niklu.
Může vyvstat otázka: co se děje s jednotlivými částicemi, jak vznikají maxima a minima při difrakci jednotlivých částic?
Experimenty na difrakci elektronových paprsků velmi nízké intenzity, tedy jakoby jednotlivých částic, ukázaly, že v tomto případě se elektron „nešíří“ různými směry, ale chová se jako celá částice. Pravděpodobnost vychýlení elektronu v určitých směrech v důsledku interakce s difrakčním objektem je však odlišná. Elektrony s největší pravděpodobností padnou do míst, která podle výpočtů odpovídají difrakčním maximům, s menší pravděpodobností padnou do míst minima. Vlnové vlastnosti jsou tedy vlastní nejen kolektivu elektronů, ale také každému elektronu jednotlivě.
4.4.2. Vlnová funkce a její fyzikální význam
Protože je mikročástice spojena s vlnovým procesem, který odpovídá jejímu pohybu, je stav částic v kvantové mechanice popsán vlnovou funkcí, která závisí na souřadnicích a čase: .
Pokud je silové pole působící na částici stacionární, tedy nezávislé na čase, pak ψ-funkce může být reprezentována jako součin dvou faktorů, z nichž jeden závisí na čase a druhý na souřadnicích:
To znamená fyzikální význam vlnové funkce:
4.4.3. Vztah nejistoty
Jedním z důležitých ustanovení kvantové mechaniky jsou vztahy neurčitosti navržené W. Heisenbergem.
Nechť se současně změří poloha a hybnost částice, přičemž nepřesnosti v určení úsečky a průmětu hybnosti na osu úsečky jsou rovny Δx, respektive Δр x.
V klasické fyzice neexistují žádná omezení, která by zakazovala současné měření jedné i druhé veličiny, tedy Δx→0 a Δр x→ 0, s jakýmkoli stupněm přesnosti.
V kvantové mechanice je situace zásadně odlišná: Δx a Δр x, odpovídající současnému určení x a р x, spolu souvisí závislostí
Volají se vzorce (4.4.8), (4.4.9). vztahy nejistoty.
Pojďme si je vysvětlit jedním modelovým experimentem.
Při studiu fenoménu difrakce byla upozorněna na skutečnost, že zmenšení šířky štěrbiny během difrakce vede ke zvětšení šířky centrálního maxima. K podobnému jevu dojde při elektronové difrakci štěrbinou v modelovém experimentu. Zmenšení šířky štěrbiny znamená zmenšení Δ x (obr. 4.4.1), což vede k většímu „rozmazání“ elektronového paprsku, tedy k větší nejistotě hybnosti a rychlosti částic.

Rýže. 4.4.1 Vysvětlení vztahu nejistoty.
Vztah nejistoty může být reprezentován jako
| , | (4.4.10) |
kde ΔE je nejistota energie určitého stavu systému; Δt je časový úsek, během kterého existuje. Vztah (4.4.10) znamená, že čím kratší je životnost kteréhokoli stavu systému, tím je jeho energetická hodnota nejistější. Energetické hladiny E 1, E 2 atd. mají určitou šířku (obr. 4.4.2)), v závislosti na době setrvání systému ve stavu odpovídajícím této úrovni.

Rýže. 4.4.2 Energetické hladiny E 1, E 2 atd. mít nějakou šířku.
„Rozostření“ hladin vede k nejistotě energie ΔE emitovaného fotonu a jeho frekvence Δν, když systém přechází z jedné energetické hladiny na druhou:
![]() ,
,
kde m je hmotnost částice; ; E a E n jsou její celkové a potenciální energie (potenciální energie je určena silovým polem, ve kterém se částice nachází, a pro stacionární případ nezávisí na čase)
Pokud se částice pohybuje pouze po určité přímce, například po ose OX (jednorozměrný případ), pak je Schrödingerova rovnice výrazně zjednodušena a má tvar
| (4.4.13) |
Jedním z nejjednodušších příkladů použití Schrödingerovy rovnice je řešení problému pohybu částic v jednorozměrné potenciálové jámě.
4.4.5. Aplikace Schrödingerovy rovnice na atom vodíku. Kvantová čísla
Popsat stavy atomů a molekul pomocí Schrödingerovy rovnice je poměrně obtížný úkol. Nejjednodušeji se to řeší pro jeden elektron umístěný v poli jádra. Takové systémy odpovídají atomu vodíku a vodíku podobným iontům (jednotlivě ionizovaný atom helia, dvakrát ionizovaný atom lithia atd.). I v tomto případě je však řešení problému složité, omezíme se proto pouze na kvalitativní představení problematiky.
Nejprve je třeba dosadit potenciální energii do Schrödingerovy rovnice (4.4.12), která pro dva interagující bodové náboje - e (elektron) a Ze (jádro) - umístěné ve vzdálenosti r ve vakuu, je vyjádřena takto:
Tento výraz je řešením Schrödingerovy rovnice a zcela se shoduje s odpovídajícím vzorcem Bohrovy teorie (4.2.30)
Obrázek 4.4.3 ukazuje úrovně možných hodnot celkové energie atomu vodíku (E 1, E 2, E 3 atd.) a graf potenciální energie E n v závislosti na vzdálenosti r mezi elektronem a jádro. S rostoucím hlavním kvantovým číslem n roste r (viz 4.2.26) a celková (4.4.15) a potenciální energie mají tendenci k nule. Kinetická energie má také tendenci k nule. Stínovaná plocha (E>0) odpovídá stavu volného elektronu.

Rýže. 4.4.3. Jsou zobrazeny úrovně možných hodnot celkové energie atomu vodíku
a graf potenciální energie versus vzdálenost r mezi elektronem a jádrem.
Druhé kvantové číslo je orbitální l, které pro dané n může nabývat hodnot 0, 1, 2, ...., n-1. Toto číslo charakterizuje orbitální moment hybnosti Li elektronu vzhledem k jádru:
Čtvrté kvantové číslo je točit m s. Může nabývat pouze dvou hodnot (±1/2) a charakterizuje možné hodnoty projekce spinu elektronů:
| .(4.4.18) |
Stav elektronu v atomu s daným n a l označujeme takto: 1s, 2s, 2p, 3s atd. Číslo zde označuje hodnotu hlavního kvantového čísla a písmeno označuje orbitální kvantové číslo: symboly s, p, d, f odpovídají hodnotám l = 0, 1, 2, 3 atd.
Kvantová mechanika je moderní teorie, která zavádí metodu popisu a zákonitostí pohybu mikročástic (elementárních částic, atomů, molekul, jader) a jejich systémů. Neobvyklost kvantově mechanických konceptů ve srovnání s klasickou fyzikou otevřela období bourání základních fyzikálních modelů, které se zdály samozřejmé a nezničitelné. To ovlivnilo především pojetí částice a principy jejího pohybu.
Tato kapitola představuje nejen kvantovou mechaniku, ale také myšlenky a experimenty, které vedly k této teorii. Elektronová mikroskopie je považována za metodu založenou na vlnových vlastnostech elektronů.
28.1. DE BROGLIEHO HYPOTÉZA. EXPERIMENTY S DIFRAKCÍ ELEKTRONŮ A JINÝCH ČÁSTIC
Důležitou etapou ve vzniku kvantové mechaniky byl objev vlnových vlastností mikročástic. Myšlenku vlnových vlastností původně předložil jako hypotézu francouzský fyzik Louis de Broglie (1924) 1 .
Po mnoho let převládala ve fyzice teorie, že světlo je elektromagnetické vlnění. Po práci Plancka (tepelné záření), Einsteina (fotoelektrický jev) a dalších se však ukázalo, že světlo má korpuskulární vlastnosti.
1 De Broglieho hypotéza byla formulována před experimenty potvrzujícími vlnové vlastnosti částic. De Broglie o tom později, v roce 1936, napsal: „... nemůžeme předpokládat, že elektron je stejně duální jako světlo? Na první pohled se tento nápad zdál velmi odvážný. Koneckonců, elektron jsme si vždy představovali jako elektricky nabitý hmotný bod, který se řídí zákony klasické dynamiky. Elektron nikdy jasně nevykazoval vlnové vlastnosti, jako je řekněme světlo v jevech interference a difrakce. Pokus připsat elektronu vlnové vlastnosti, když pro to neexistují žádné experimentální důkazy, by mohl vypadat jako nevědecká fantazie.
V kap. 24 bylo zaznamenáno, že na krystalických tělesech je pozorována rentgenová difrakce; Proto je pro elektronovou difrakci nutné používat i krystalické látky.
K. Davisson a L. Germer poprvé pozorovali difrakci elektronů z monokrystalu niklu, J.P. Thomson a nezávisle na něm P.S. Tartakovsky - na kovové fólii (polykrystalické tělo).
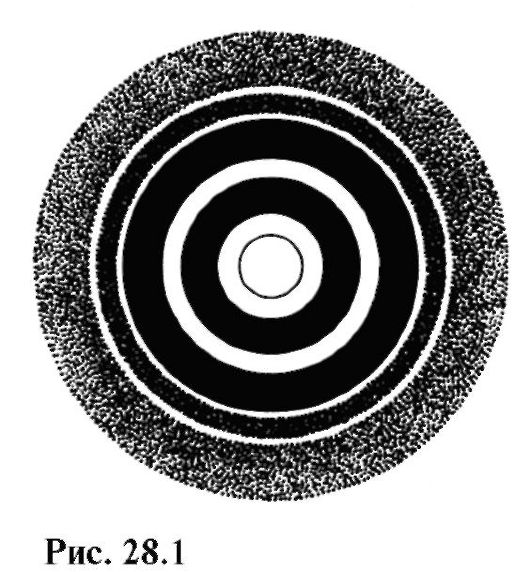
Na Obr. Obrázek 28.1 ukazuje elektrongram - difrakční obrazec získaný z interakce elektronů s polykrystalickou fólií.
Porovnáním tohoto obrázku s Obr. 24.21 si lze všimnout podobnosti mezi difrakcí elektronů a rentgenovým zářením.
Schopnost difrakce mají i další částice, jak nabité (protony, ionty atd.), tak neutrální (neutrony, atomy, molekuly).
Podobně jako u rentgenové difrakční analýzy lze difrakci částic použít k určení uspořádaného nebo neuspořádaného uspořádání atomů a molekul látky ak odhadu parametrů krystalových mřížek.
V současné době jsou široce používány metody elektronové difrakce (elektronová difrakce) a neutronové difrakce (neutronová difrakce).
Mohou vyvstat otázky: co se děje s jednotlivými částicemi, jak vznikají maxima a minima při difrakci jednotlivých částic?
Experimenty na difrakci elektronových paprsků velmi nízké intenzity, tzn. jako by šlo o samostatné částice, ukázal, že v tomto případě se elektron „nešíří“ různými směry, ale chová se jako celá částice. Pravděpodobnost vychýlení elektronu v určitých směrech v důsledku interakce s difrakčním objektem je však odlišná. Elektrony s největší pravděpodobností padnou do míst, která podle výpočtů odpovídají difrakčním maximům, s menší pravděpodobností padnou do míst minima. Vlnové vlastnosti jsou tedy vlastní nejen kolektivu elektronů, ale také každému elektronu jednotlivě.
28.2. ELEKTRONOVÝ MIKROSKOP. KONCEPCE ELEKTRONICKÉ OPTIKY
Vlnové vlastnosti částic lze využít nejen pro difrakční strukturní analýzu, ale také pro získání zvětšených snímků objektu.
Z (26.19) vyplývá, že mez rozlišení optického mikroskopu určuje především mezní hodnota vlnové délky světla vnímaného lidským okem. Dosazením hodnoty de Broglieho vlnové délky (28.3) do tohoto vzorce najdeme mez rozlišení elektronového mikroskopu, ve kterém je obraz předmětu tvořen elektronovými paprsky:
Jak je snadno vidět, limit rozlišení z Elektronový mikroskop závisí na urychlovacím napětí a lze dosáhnout toho, že je mnohem nižší a rozlišovací schopnost mnohem větší než u optického mikroskopu.
Elektronový mikroskop a jeho jednotlivé prvky jsou svým účelem podobné optickému mikroskopu, proto použijeme přirovnání k vysvětlení jeho struktury a principu činnosti. Schémata obou mikroskopů jsou na Obr. 28,2 (a - optický; b - elektronický).
V optickém mikroskopu nositel informace o objektu AB je foton, světlo. Zdrojem světla bývá žárovka /. Po interakci s objektem (absorpce, rozptyl, difrakce) se proud fotonů transformuje a obsahuje informace o objektu. Fotonový tok se tvoří pomocí optických zařízení, především čoček: kondenzor 3, objektiv 4, okulár 5. Obraz A 1 B 1 je zaznamenáván okem 7 (nebo fotografickou deskou, fotoluminiscenčním stínítkem apod.).
V elektronovém mikroskopu je nositelem informace o předmětu elektron a zdrojem elektronů je žhavená katoda 1. Urychlování elektronů a vznik paprsku provádí fokusační elektroda a anoda - systém tzv. elektronové dělo 2. Po interakci s objektem (hlavně rozptylu) se tok elektronů transformuje a obsahuje informace o subjektu. Ke vzniku toku elektronů dochází vlivem elektrického pole (systém elektrod a kondenzátorů) a magnetického pole (systém

ma cívky s proudem). Tyto systémy se nazývají elektronické čočky analogicky s optickými čočkami, které tvoří světelný tok (3 - kondenzátor; 4 - elektronické, sloužící jako čočka, 5 - projekce). Obraz je zaznamenán na elektronově citlivou fotografickou desku nebo katodoluminiscenční stínítko 6.
Pro odhad meze rozlišení elektronového mikroskopu dosadíme do vzorce (28.4) urychlovací napětí 100 kV a úhlovou aperturu řádově 10 -2 rad (přibližně tyto úhly se používají v elektronové mikroskopii). Pak dostaneme z ~ 0,1 nm, což je stokrát lepší než u optických mikroskopů. Použití urychlovacího napětí většího než 100 kV, přestože zvyšuje rozlišení, je spojeno s určitými obtížemi, zejména se vyskytuje
zničení studovaného objektu elektrony s vysokou rychlostí. V praxi je i s nejlepším elektronovým mikroskopem možné dosáhnout hranice rozlišení řádově 10 -10 m; to je stokrát lepší než optické mikroskopy.
Mezi výhody elektronového mikroskopu patří vysoká rozlišovací schopnost umožňující zkoumání velkých molekul, možnost v případě potřeby měnit urychlovací napětí a následně i mez rozlišení a poměrně pohodlné řízení toku elektronů pomocí magnetických a elektrických polí.
Uveďme některé rysy činnosti elektronového mikroskopu. V těch jeho částech, kde létají elektrony, musí být vakuum, protože jinak srážka elektronů s molekulami vzduchu (plynu) povede ke zkreslení obrazu. Tento požadavek na elektronovou mikroskopii komplikuje výzkumný postup a činí zařízení těžkopádnějším a nákladnějším. Vakuum narušuje přirozené vlastnosti biologických objektů a v některých případech je ničí nebo deformuje.
Pro zkoumání pod elektronovým mikroskopem jsou vhodné pouze velmi tenké řezy, protože elektrony jsou látkou silně absorbovány a rozptylovány. Proto je v některých případech vhodné otisknout povrch studovaného předmětu na tenkou vrstvu plastu. Tento postup se nazývá replikace a nazývá se plastická kopie povrchu replika.

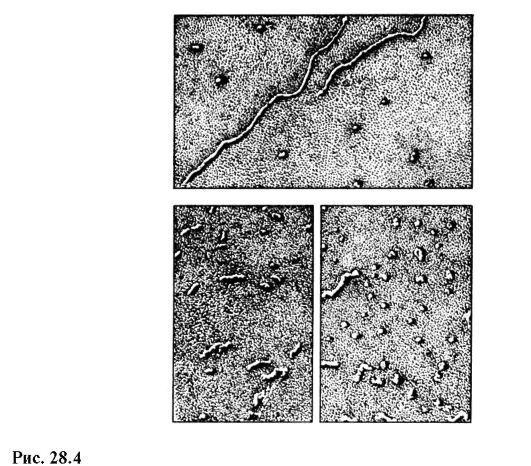
Moderní domácí elektronový mikroskop EVM-100 LM (obr. 28.3) poskytuje maximální zvětšení 600 000x a garantovaný limit rozlišení 3? 10 -10 m. Obr. Obrázek 28.4 ukazuje fotografie molekul RNA v různých stavech získané na elektronovém mikroskopu se 100 000násobným zvětšením.
Přítomnost vlnových a korpuskulárních vlastností jak u fotonů, tak elektronů a dalších částic umožňuje řadu ustanovení a zákonů optiky rozšířit i na popis pohybu nabitých částic v elektrických a magnetických polích.
Tato analogie umožnila identifikovat se jako samostatný oddíl elektronická optika - obor fyziky, ve kterém se studuje struktura svazků nabitých částic interagujících s elektrickými a magnetickými poli. Stejně jako konvenční optiku lze elektronickou optiku rozdělit na geometrický (radiální) a vlna(fyzikální).
V rámci geometrické elektronové optiky je popsán zejména pohyb nabitých částic v elektrických a magnetických polích. Schematické znázornění konstrukce obrazu v elektronovém mikroskopu (viz obr. 28.2, b) je založeno na geometrické elektronové optice.
Přístup vlnové elektronové optiky je zásadní v případě, kdy se objevují vlnové vlastnosti nabitých částic. Dobrým příkladem je zjištění rozlišení (limit rozlišení) uvedeného na začátku odstavce.
28.3. VLNOVÁ FUNKCE A JEJÍ FYZIKÁLNÍ VÝZNAM
Protože je mikročástice spojena s vlnovým procesem, který odpovídá jejímu pohybu, je stav částic v kvantové mechanice popsán vlnovou funkcí závislou na souřadnicích a čase: ψ(χ, y, z, t).
Je-li silové pole působící na částici stacionární, tzn. nezávisle na čase, pak ψ-funkce může být reprezentována jako součin dvou faktorů, z nichž jeden závisí na čase a druhý na souřadnicích:
V následujícím budeme uvažovat pouze stacionární stavy; ψ-funkce je pravděpodobnostní charakteristika stavu částice. Pojďme si vysvětlit význam tohoto tvrzení.
Zvolme dostatečně malý objem v prostoru dPROTI= dxdjdz, v rámci kterého lze hodnoty ψ-funkce považovat za identické. Pravděpodobnost nálezu dW Bčástice v tomto objemu jsou úměrné objemu a závisí na kvadrátu modulu ψ-funkce:

Kvadratický modul vlnové funkce je roven hustotě pravděpodobnosti, tzn. poměr pravděpodobnosti nalezení částice v objemu k tomuto objemu.
Integrováním výrazu (28.6) přes určitý objem V zjistíme pravděpodobnost nalezení částice v tomto objemu:
28.4. VZTAHY NEJISTOTY
Jedním z důležitých ustanovení kvantové mechaniky jsou vztahy neurčitosti navržené W. Heisenbergem.
Nechť se současně změří poloha a hybnost částice, přičemž nepřesnosti v určení úsečky a průmětu hybnosti na osu úsečky jsou rovny Δχ, respektive Δр x.

1 Ve skutečnosti není možné takový experiment provést, protože rozměry mezery musí být v řádu atomů, takže je popsán určitý myšlenkový experiment.

Řešení (28.11) znamená, že čím kratší je životnost kteréhokoli stavu systému, tím je jeho energetická hodnota nejistější. Energetické hladiny E 1, E 2 atd. mají určitou šířku (obr. 28.6), v závislosti na době setrvání systému ve stavu odpovídajícím této úrovni.
„Rozostření“ úrovní vede k nejistotě energie AE emitovaného fotonu a jeho frekvence Ay, když systém přechází z jedné energetické úrovně na druhou:
Vzhledem k tomu, že stav mikročástice je popsán pomocí ψ-funkce, je nutné uvést způsob zjištění této funkce s přihlédnutím k vnějším podmínkám. To je možné díky řešení základní rovnice kvantové mechaniky navržené E. Schrödingerem (1926). Taková rovnice je postulována v kvantové mechanice stejným způsobem, jako je postulován druhý Newtonův zákon v klasické mechanice.
Ve vztahu ke stacionárním stavům lze Schrödingerovu rovnici napsat takto:
To se projevuje rozšířením spektrálních čar.
28.5. SCHRÖDINGEROVA ROVNICE. ELEKTRON V POTENCIÁLNÍ DOBŘE
Kde m- hmotnost částic; E a E p - jeho celková a potenciální energie (potenciální energie je určena silovým polem, ve kterém se částice nachází, a pro stacionární případ nezávisí na čase).
Pokud se částice pohybuje pouze po určité přímce, například po ose X(jednorozměrný případ), pak je Schrödingerova rovnice výrazně zjednodušena a má tvar:
Jedním z nejjednodušších příkladů použití Schrödingerovy rovnice je řešení problému pohybu částic v jednorozměrné potenciálové jámě.
Nechte elektron pohybovat se podél osy X pouze v rozmezí 0< X < l(obr. 28.7). To znamená, že v zadaném intervalu je ψ-funkce nenulová a mimo interval (x<0, X>l) se rovná nule.
Protože silová pole ve zvoleném intervalu na částici nepůsobí, může mít její potenciální energie libovolnou konstantní hodnotu (nejvhodnější je vzít E p= 0). Mimo tento interval není žádný elektron, takže jeho potenciální energie by měla být považována za nekonečně velkou. Na Obr. Obrázek 28.7 ukazuje grafickou závislost E p = D x). Interval 0< X < l, удовлетворяющий сформулированным выше условиям, называют одномерной прямоугольной потенциальной ямой с бесконечно высокими стенками. С учетом E p= 0 Schrödingerova rovnice (28.14) pro interval 0< X < l má tvar:

Tato rovnice je podobná diferenciální rovnici harmonického kmitání (viz 7.1), jejíž řešení je:

Především je pozoruhodné, že řešení Schrödingerovy rovnice pro elektron v potenciálové jámě bez dalších postulátů vede k diskrétním, kvantovaným energetickým hodnotám:

Z (28.21) je zřejmé, že pro nějakou pevnou hodnotu n diskrétnost, tzn. Čím větší je velikost potenciální studny, tím menší je rozdíl energií sousedních hladin. Spočítejme tedy například dva případy s n = 1:
1) l= 5? 10 -10 m, což přibližně odpovídá velikosti atomu; Pak ΔΕ = 4,5 eV. To se řádově shoduje s hodnotami získanými pro atom vodíku podle Bohrovy teorie;
2) l= 10 -1 m, což vlastně odpovídá takové šířce potenciálové jámy, že elektron lze považovat za volný; ve stejnou dobu ΔΕ = 1.1? 10-16 eV. Zde je diskrétnost zanedbatelná a prakticky lze předpokládat, že energie elektronu se plynule mění.
Umocněním (28.20) získáme hustotu pravděpodobnosti |ψ| 2 nalezení elektronu v různých bodech potenciálové jámy. Na Obr. Obrázek 28.9 ukazuje grafickou závislost |ψ| 2 od χ v různých diskrétních stavech, tzn. různá kvantová čísla. Jak je z obrázku patrné, elektron se může nacházet na různých místech v potenciálové jámě s různou pravděpodobností. Jsou body, ve kterých je pravděpodobnost nalezení elektronu nulová. To se výrazně liší od koncepcí klasické fyziky, podle kterých je přítomnost částice na různých místech potenciální jámy stejně pravděpodobná (obr. 28.10) a nelze ji rozdělit podle bodů, ve kterých přítomnost částice je vyloučeno.
Schrödingerovu rovnici lze aplikovat i na složitější silová pole, jako je elektron v atomu. To povede k dalším matematickým potížím, ale nezmění to hlavní rysy

atomové systémy: diskrétnost energetických stavů, pravděpodobnostní soudy o umístění elektronu, zvláštní závislost |ψ| 2 ze souřadnic atd.
28.6. APLIKACE SCHRÖDINGEROVY ROVICE NA ATOM VODÍKU. KVANTOVÁ ČÍSLA
Popsat stavy atomů a molekul pomocí Schrödingerovy rovnice je poměrně obtížný úkol. Nejjednodušeji se to řeší pro jeden elektron umístěný v poli jádra. Takové systémy odpovídají atomu vodíku a vodíku podobným iontům (jednotlivě ionizovaný atom helia, dvakrát ionizovaný atom lithia atd.). Řešení problému je však i v tomto případě nad rámec našeho kurzu, a tak se omezíme pouze na kvalitativní představení problematiky.
Nejprve je třeba dosadit potenciální energii do Schrödingerovy rovnice (28.13), která pro dva interagující bodové náboje je E(elektron) a Ze(jádro), - umístěné na dálku r ve vakuu se vyjadřuje takto:
Vzhledem ke středové symetrii pole vytvořeného jádrem je vhodnější problém řešit nikoli v kartézských pravoúhlých souřadnicích, ale ve sférických r, θ a p.
Řešení Schrödingerovy rovnice se nalézá jako součin tří funkcí, z nichž každá závisí na jedné proměnné:
Stejně jako u elektronu v pravoúhlé potenciálové jámě s nekonečně vysokými stěnami vedly okrajové podmínky ke konkrétním možným hodnotám ψ a energie, tak v potenciálové jámě odpovídající atomu vodíku vedou fyzikální podmínky k možným hodnotám f1, f 2, f 3 a odtud ψ-funkce. Projevuje se zde i hlavní rys kvantově mechanických systémů - diskrétnost stavů.
Diskrétnost matematicky spočívá v tom, že kterákoli z funkcí rovnice (28.23) má celou množinu (spektrum) řešení, z nichž každé odpovídá určitému kvantovému číslu. Na rozdíl od pravoúhlé potenciálové jámy s nekonečně vysokými stěnami je stav elektronu v atomu charakterizován nikoli jedním, ale několika kvantovými čísly 1 . První je hlavní kvantové číslo p - 1, 2, 3... Určuje energetické hladiny elektronu podle zákona:

Tento výraz je řešením Schrödingerovy rovnice a zcela se shoduje s odpovídajícím vzorcem Bohrovy teorie (viz 28.7).
Na Obr. Obrázek 28.11 ukazuje úrovně možných hodnot celkové energie atomu vodíku (E 1, E 2, E 3 atd.) a graf potenciální energie E P v závislosti na vzdálenosti r mezi elektronem a jádrem [viz (28,22)]. S rostoucím hlavním kvantovým číslem n zvyšuje r[viz například (28.33)] a doplňte [viz. (28.24)] a potenciální energie má tendenci k nule. Kinetická energie má také tendenci k nule. Stínovaná plocha (E >0) odpovídá stavu volného elektronu.
1 Obecně jsou kvantová čísla celočíselná (0, 1, 2...) nebo poloviční celá (1/2, 3/2, 5/2...) čísla, která definují možné diskrétní hodnoty fyzikálních veličin, které charakterizovat kvantové systémy a elementární částice.

1 Přítomnost spinu v částicích nevyplývá ze Schrödingerovy rovnice.
s tímto výpočtem: strávila více času na místech s vyšší hustotou pravděpodobnosti, méně času na místech s nižší hustotou pravděpodobnosti. V důsledku expozice na fotografický film byly získány oblasti různé intenzity, které ilustrují rozložení elektronu v atomu. Z obrázků je zřejmé, jak svévolný a dokonce nesprávný je pojem „orbita“ ve vztahu k pohybu elektronu.
Spin a orbitální magnetické momenty se vzájemně ovlivňují, což mění systém energetických hladin atomu ve srovnání s tím, jaký by byl bez takové interakce. Říká se, že interakce spin-orbita vedou k jemné struktuře energetických hladin. Pokud je významný, pak je nutné vzít v úvahu celkový moment hybnosti elektronu - orbital plus spin. Navíc místo toho m l A m s použijte jiná kvantová čísla: j A nij.
Kvantové číslo j- orbital plus spin - určuje diskrétní hodnoty celkového momentu hybnosti L elektron:

Magnetické kvantové číslo m) charakterizuje možné průměty celkového momentu hybnosti do nějakého libovolně zvoleného směru Z:
Pro daný l kvantové číslo j nabývá dvou hodnot: ±1/2
(Tabulka 28.1).
Tabulka 28.1

Pro daný j kvantové číslo nij nabývá hodnot 2j + 1: -j, -j + 1 ... + j.
28.7. KONCEPCE O BOHR TEORIE
Ještě před vytvořením kvantové mechaniky v roce 1913 navrhl dánský fyzik N. Bohr teorii atomu vodíku a vodíku podobných iontů, která byla založena na jaderném modelu atomu a jeho dvou postulátech. Bohrovy postuláty nezapadaly do rámce klasické fyziky.
Podle prvního postulátu mohou atom a atomové systémy setrvat pouze v určitých stacionárních stavech po dlouhou dobu. V takových stavech atom nevyzařuje ani neabsorbuje energii. Stacionární stavy odpovídají diskrétním energetickým hodnotám: E 1, E 2...
Jakákoli změna energie atomu nebo atomového systému je spojena s náhlým přechodem z jednoho stacionárního stavu do druhého.
Podle druhého postulátu při přechodu atomu z jednoho stavu do druhého atom emituje nebo absorbuje foton, jehož energie je určena rovnicí (29.1).
Přechod ze stavu s vyšší energií do stavu s nižší energií je doprovázen emisí fotonu. Opačný proces je možný, když je foton absorbován.
Podle Bohrovy teorie se elektron v atomu vodíku otáčí po kruhové dráze kolem jádra. Stacionární stavy ze všech možných drah odpovídají pouze těm, pro které je moment hybnosti roven celému číslu h/(2π):
(n = 1, 2, 3...), (28,31)
Kde m- elektronová hmotnost; υ η - jeho rychlost na n-té oběžné dráze; rn- jeho poloměr. Elektron rotující po kruhové dráze v atomu je vystaven Coulombově přitažlivé síle kladně nabitého jádra, která se podle druhého Newtonova zákona rovná součinu hmotnosti elektronu a dostředivého zrychlení (zápis uvedený pro vakuum ):

Navzdory velkému úspěchu Bohrovy teorie byly brzy patrné její nedostatky. V rámci této teorie tedy nebylo možné vysvětlit rozdíl v intenzitách spektrálních čar, tzn. odpovědět na otázku, proč jsou některé energetické přechody pravděpodobnější než jiné. Bohrova teorie neodhalila spektrální vzorce složitějšího atomového systému – atomu helia (dva elektrony rotující kolem jádra).
Nevýhodou Bohrovy teorie byla její nejednotnost. Tato teorie nebyla ani klasická, ani kvantová, kombinovala ustanovení zásadně odlišných teorií: klasické a kvantové fyziky. Takže například v Bohrově teorii se věří, že elektron rotuje v atomu po určité dráze (klasické koncepty), ale zároveň nevyzařuje elektromagnetickou vlnu (kvantové koncepty).
V první čtvrtině tohoto století se ukázalo, že Bohrova teorie musí být nahrazena jinou teorií atomu. Objevila se kvantová mechanika.
28.8. ELEKTRONOVÉ PLÁŠŤY KOMPLEXNÍCH ATOMŮ
Kvantová čísla, která popisují stav elektronu v atomu vodíku, se používají k přiblížení stavu jednotlivých elektronů ve složitých atomech. Je však třeba vzít v úvahu alespoň dva významné rozdíly mezi komplexními atomy a atomem vodíku:
1) ve složitých atomech závisí energie elektronů v důsledku jejich interakce nejen na n, ale také na /;
2) rozdíl je způsoben Pauliho principem, podle kterého atom nemůže mít dva (nebo více) elektronů se čtyřmi stejnými kvantovými čísly.
Když se vytvoří elektronová konfigurace odpovídající normálnímu stavu, každý elektron atomu má tendenci mít nejnižší energii. Nebýt Pauliho principu, pak by se všechny elektrony nacházely na nejnižší energetické úrovni. Ve skutečnosti, s některými výjimkami, elektrony zaujímají sekvenci stavů označenou pro atom vodíku v tabulce. 29.
Elektrony se stejným hlavním kvantovým číslem tvoří vrstvu. Vrstvy se nazývají NA, L, M, N atd. v souladu s n= 1, 2, 3, 4... Elektrony se stejnými páry hodnot n A / , jsou součástí obalu, který je stručně označen stejně jako odpovídající stavy pro elektron atomu vodíku: 1s, 2s, 2^ atd. Takže například nazývají obal 2s, elektrony 2s atd.
Počet elektronů v obalu je uveden vpravo nahoře vedle symbolického označení obalu, například 2p 4.
Rozložení elektronů mezi obaly v atomu (elektronické konfigurace) se obvykle označuje takto: pro dusík 1s 2, 2s 2, 2p 3, pro vápník 1s 2, 2s 2, 2p 6, 3s 2, 3p 6, 4s 2 atd.
Protože energie elektronu komplexních atomů závisí nejen na n, ale také na l, pak ke konstrukci periodické tabulky nedochází vždy postupným zaplňováním vrstev, jak se atom stává složitějším. V draslíku (Z = 19), například místo vyplnění vrstvy M(možná tam byly 1s 2, 2s 2, 2^6, 3s 2, 3p 6, 3a 1) začíná plnění vrstvy N a vytvoří se následující elektronická konfigurace: 1 s2, 2s 2, 2р 6, 3 s 2, 3p 6, 4 s 1.
Podobné odchylky od pravidelného plnění vrstev existují i u dalších prvků.
Vždy se dodržuje obecné pravidlo: elektrony nevybuzeného atomu zaujímají stav s nejnižší energií a v souladu s Pauliho principem. Na Obr. Obrázek 28.13 schematicky ukazuje, bez ohledu na měřítko, energetické stavy komplexního atomu a odpovídající počet elektronů.
Na závěr poznamenáváme, že stav multielektronového atomu jako celku je určen následujícími kvantovými čísly: L- celkový orbitální moment atomu, který nabývá hodnot 0, 1, 2, 3 atd. 1; J- celkový moment atomu, který může nabývat hodnot s intervalem jedna od |L - S| na |L + S |; S- výsledný spinový moment atomu; magnetický m J, který určuje diskrétní hodnoty průmětu celkového momentu atomu na určitou osu Z:

Pro daný Jm J bere 2 J+ 1 hodnoty:
-J, -J+ 1 ... +J.
1 Toto označení by se nemělo zaměňovat s názvem elektronické vrstvy L a s celkovým momentem hybnosti elektronu.
28.9. ENERGETICKÉ HLADINY MOLEKUL
Protože molekuly jsou tvořeny atomy, intramolekulární pohyb je složitější než intraatomický pohyb. V molekule kromě pohybu elektronů vzhledem k jádrům dochází k vibračnímu pohybu atomů kolem jejich rovnovážné polohy (vibrace jader spolu s elektrony, které je obklopují) a k rotačnímu pohybu molekuly jako celku.
Elektronické, vibrační a rotační pohyby molekuly odpovídají třem typům energetických úrovní: Eel, Ecol a Etemp. Podle kvantové mechaniky nabývá energie všech typů pohybu v molekule pouze diskrétní hodnoty (kvantované). Představme přibližně celkovou energii E molekuly součtem kvantovaných energií různých typů:
E= E el + E počet + E čas.
(28,37) Na Obr. 28.14 schematicky znázorňuje systém hladin molekuly: daleko od sebe hladiny elektronické energie A" Na Obr. 28.14 schematicky znázorňuje systém hladin molekuly: daleko od sebe hladiny elektronické energie A ", pro které E coll = E vr = 0; blíže umístěné vibrační úrovně , ", pro které E coll = E vr = 0; blíže umístěné vibrační úrovně proti" ", pro ně E vr = 0; nejblíže umístěné rotační úrovně A" J" J""
s různými hodnotami času E.

Vzdálenost mezi elektronickými energetickými hladinami je v řádu několika elektronvoltů, mezi sousedními vibračními hladinami 10-2-10-1 eV, mezi sousedními rotačními hladinami 10-5-10-3 eV.
Již víme, že v optických jevech je pozorován jakýsi dualismus. Spolu s jevy difrakce a interference (vlnové jevy) jsou pozorovány i jevy, které charakterizují korpuskulární povahu světla (fotoelektrický jev, Comptonův jev).
V roce 1924 to předpokládal Louis de Broglie dualismus není rysem pouze optických jevů ,ale má univerzální charakter. Částice hmoty mají také vlnové vlastnosti .
„V optice,“ napsal Louis de Broglie, „byla po celé století korpuskulární metoda vyšetření příliš opomíjena ve srovnání s vlnovou; neudělala se v teorii hmoty opačná chyba?" Za předpokladu, že částice hmoty spolu s korpuskulárními vlastnostmi mají také vlnové vlastnosti, de Broglie přenesl na případ částic hmoty stejná pravidla přechodu z jednoho obrázku do druhého, která platí v případě světla.
Pokud má foton energii a hybnost, pak částice (například elektron) pohybující se určitou rychlostí má vlnové vlastnosti, tzn. pohyb částice lze považovat za pohyb vlny.
Podle kvantové mechaniky volný pohyb částice s hmotností m a hybnost (kde υ je rychlost částice) může být reprezentována jako rovinná monochromatická vlna ( de Broglieho vlna) s vlnovou délkou
| (3.1.1) |
šířící se ve stejném směru (například ve směru osy X), ve kterém se částice pohybuje (obr. 3.1).

Závislost vlnové funkce na souřadnici X je dáno vzorcem
| , | (3.1.2) |
kde - vlnové číslo ,A vlnový vektor směřující k šíření vlny nebo podél pohybu částice:
| . | (3.1.3) |
Tedy, monochromatický vlnový vektor spojené s volně se pohybujícími mikročásticemi, úměrné jeho hybnosti nebo nepřímo úměrné vlnové délce.
Protože kinetická energie relativně pomalu se pohybující částice je , lze vlnovou délku vyjádřit také energií:
| . | (3.1.4) |
Když částice interaguje s nějakým předmětem - s krystalem, molekulou atd. – mění se její energie: k ní se přidává potenciální energie této interakce, což vede ke změně pohybu částice. Podle toho se mění povaha šíření vlny spojené s částicí, a to se děje podle principů společných všem vlnovým jevům. Proto se základní geometrické obrazce difrakce částic neliší od obrazců difrakce jakýchkoliv vln. Obecnou podmínkou pro difrakci vlnění jakékoli povahy je souměřitelnost délky dopadající vlny λ se vzdáleností d mezi rozptylovými centry: .
Hypotéza Louise de Broglieho byla revoluční, dokonce i na tu revoluční dobu ve vědě. Brzy to však bylo potvrzeno mnoha experimenty.
KLASICKÉ MODELY ATOM A JEJICH NEVÝHODY.
Nápady o čem atomy nejsou nedělitelné částice a obsahují jako složky
elementární náboje částic byly nejprve vyjádřeny na konciXIX století Termín „elektron“ navrhl v roce 1881 anglický fyzik GeorgeSténání. V roce 1897 byla elektronová hypotéza experimentálně přijatapotvrzení ve studiích Emila Wicherta a Josepha Jana Thomsona. Od tohoto okamžiku začala tvorba různých elektronických modelůatomů a molekul.Thomsonův první model předpokládal, že kladný náboj je jednotnýrozptýlené v atomu a do něj, jako rozinky v housce,elektrony jsou rozptýleny.Rozpor mezi tímto modelem a experimentálními daty se ukázal být jasnýpo experimentu v roce 1906 Ernestem Rutherfordem, který vyšetřoval
proces rozptylu částic alfa atomy. Ze zkušenosti, kterou jste udělali,že kladný náboj je koncentrován uvnitř útvaru, je podstatnémenší než velikost atomu. Tento útvar se nazýval atomovýjádro, jehož rozměry byly 1 o-12 cm a rozměry atomu byly 1 o-v cm.
V souladu s klasickými koncepty elektromagnetismumezi každým elektronem a jádrem musí být Coulombova sílaatrakce. Závislost této síly na vzdálenosti by měla být následujícístejně jako v zákonu univerzální gravitace. Proto ten pohyb
elektrony v atomu by měly být podobnéale pohyb planet sluneční soustavy.Tak se zrodil planetární modelRutherfordův atom.Další výzkum udržitelnostiatom dal ohromující výsledek:výpočty ukázaly, že během1 o-9 s musí elektron dopadnout k jádru
kvůli ztrátě energie v důsledku záření. Navíc takový model dalkontinuální spíše než diskrétní emisní spektra atomů.
TEORIE ATOMU BÓRU.
Dalším důležitým krokem v Vývoj teorie atomů provedl Niels Bohr.
Nejdůležitější hypotéza předložená Bohrem v V roce 1913 se objevila hypotéza o diskrétní struktuře
energetické hladiny elektronu v atomu. Tato pozice ilustrovaný na energii
diagramy. Tradičně na energii diagramech, energie je uložena vertikálně
osy Rozdíl mezi pohybem tělesa v gravitačním poliz pohybu elektronu v atomuv souladu s Bohrovou hypotézou se skládá zže energie těla se může neustále měnit,a energie elektronů v záporných hodnotáchmůže nabývat řady diskrétních hodnot,znázorněno na obrázku segmenty modrébarvy. Tyto diskrétní hodnoty byly tzvenergetické hladiny nebo jinými slovy energieúrovně. Samozřejmě, myšlenka diskrétních úrovní energiebyl převzat z Planckovy hypotézy. Změna energieelektron v souladu s Bohrovou teorií mohlvyskytují se pouze ve skocích (z jedné energetické hladiny k jinému). Bohrova teorie dokonale vysvětlila lineární charakter
atomová spektra. Když se však zeptali na důvod diskrétnosti
úrovně, teorie ve skutečnosti neposkytla odpověď.
VLNY HMOTY.
Dalším krokem ve vývoji teorie mikrosvěta byl vytvořil Louis de Broglie. V roce 1924 to navrhlpohyb mikročástic by neměl být popisován jako klasický mechanický
pohyb, ale jako nějaký vlnový pohyb. Vyplývá to ze zákonů vlnění, je třeba získat recepty na výpočet rozdílůžádné pozorovatelné veličiny. Takže ve vědě spolu s elektromagnetickými vlnamipole, objevily se vlny hmoty.Hypotéza o vlnové povaze pohybu částic byla stejně odvážná jakostejně jako Planckova hypotéza o vlastnostech diskrétního pole. Experimentovat,přímo potvrzující hypotézuBroglie, byl dodán až v roce 1927.V tomto experimentu to bylo pozorovánoelektronová difrakce na krystalu,podobně jako elektromagnetická difrakce vlny. Hypotéza o vlnách hmoty byla povolenavysvětlit diskrétní povahu
energetické hladiny. Z teorie vlny, bylo známo, že vlna omezená prostorem má vždydiskrétní frekvence. Příkladem je vlna v takovém muzikálunástroj jako flétna. Frekvence zvuku je v tomto případě určenarozměry prostoru, kterým je vlna omezena (rozměry flétny).Ukazuje se, že jde o obecnou vlastnost vlnění.Ale v souladu s Planckovou hypotézou, frekvence elektromagnetického kvantavlny jsou úměrné energii kvanta. V důsledku toho energie elektronůmusí nabývat diskrétních hodnot.De Broglieho nápad se ukázal jako velmi plodný, i když, jak již bylo zmíněno,přímý experiment potvrzující vlnové vlastnosti elektronu, byla provedena až v roce 1927. V roce 1926 Erwin Schrödinger odvodil rovnici,kterému se musí elektronová vlna podřídit, a když se rozhodlo totorovnice aplikovaná na atom vodíku, získala všechny výsledky, kteréBohrova teorie byla schopna poskytnout. Ve skutečnosti to byl začátekmoderní teorie popisující procesy v mikrokosmu, od rvlnová rovnice byla snadno zobecněna pro širokou škálu systémů - multielektronatomy, molekuly, krystaly.Vývoj teorie vedl k pochopení, že vlna odpovídáčástice, určuje pravděpodobnost nalezení částice v daném boděplocha. Tak vstoupil pojem pravděpodobnosti do fyziky mikrosvěta.Podle nové teorie vlna odpovídající částici zcela určujepohyb částic. Ale obecné vlastnosti vlnění jsou takové, že vlněnínelze lokalizovat v žádném bodě prostoru, tzn. nesmyslnémluvit o souřadnicích částice v daném časovém okamžiku.Důsledkem toho bylo úplné vyloučení z fyziky mikrosvěta takovýchkoncepty, jako je trajektorie částic a oběžné dráhy elektronůatom. Krásný a vizuální planetární model atomu, jak se ukázalo,
- Podání elektronického hlášení finančnímu úřadu přes internet
- Vyloučení právnické osoby z Jednotného státního rejstříku za nepravdivé informace: důvody, odvolání proti rozhodnutí Federální daňové služby o nadcházejícím vyloučení
- Co je to hostinec, můžete to zjistit kontaktováním pověřeného orgánu
- Žádost o zrušení registrace UTII IP Důvody zrušení registrace UTII
